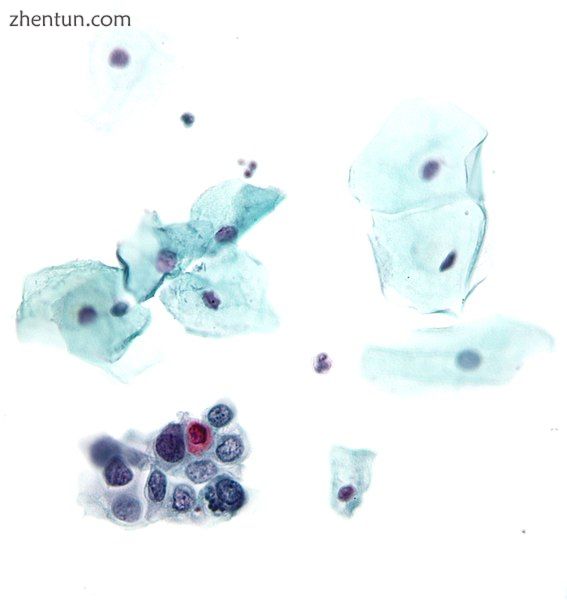
高度鳞状上皮内病变
Papanicolaou测试(缩写为Pap测试,也称子宫颈抹片检查,子宫颈涂片,宫颈透视或涂片测试)是一种宫颈筛查方法,用于检测子宫颈中可能的癌前和癌变过程(子宫或子宫的开放) )。异常发现通常随后采用更敏感的诊断程序,如果有必要,可采取旨在预防宫颈癌发展的干预措施。该测试由医生AurelBabeş和医生Georgios Papanikolaou发明并命名。
通过用窥器打开阴道腔进行子宫颈抹片检查,然后在转化区(外部鳞状宫颈细胞与内腺体宫颈内细胞相遇)处收集宫颈外开口处的细胞。在显微镜下检查收集的细胞以寻找异常。该试验旨在检测潜在的癌前变化(称为宫颈上皮内瘤变(CIN)或宫颈发育不良;鳞状上皮内病变系统(SIL)也用于描述异常),这是由人乳头瘤病毒(一种性传播的DNA病毒)引起的。 该试验仍然是一种有效的,广泛使用的早期检测癌症前期和宫颈癌的方法。虽然该测试还可以检测宫颈内膜和子宫内膜的感染和异常,但并不是这样设计的。
在美国,建议从21岁左右开始进行子宫颈抹片检查,直至65岁。但是,其他国家不建议对非性活跃的女性进行pap检测。频率指南每三到五年不等。如果结果异常,并且根据异常的性质,可能需要在6到12个月内重复测试。如果异常需要更仔细的检查,可以通过阴道镜检查转诊患者以详细检查子宫颈。该人员也可以转诊进行HPV DNA检测,该检测可作为Pap检测的辅助手段。可以作为巴氏试验的辅助试验应用的其他生物标志物正在发展。
目录
1 医疗用途
1.1 有效性
1.2 结果
1.3 怀孕
2 程序
2.1 自动分析
2.2 筛选类型
2.3 实践方面
3 历史
4 实验技术
5 访问
6 球菌细菌
7 参考文献
医疗用途
女性在开始筛查之前应该在第一次性交后等待几年,并且不应该在21岁之前进行筛查。美国妇产科医师大会(ACOG)和其他人建议在21岁时开始筛查(从那以后几年)大多数美国女性的初始性行为)。许多其他国家等到25岁或更晚才开始筛查。例如,英国的一些地方在25岁开始筛查.ACOG的一般建议是,年龄在30-65岁的人有一年一次的妇女检查,他们没有接受年度巴氏试验,并且她们确实接受了巴氏试验。三年间隔。
HPV通过皮肤接触皮肤;虽然性传播是一种常见的方式,但性并不一定要发生。它需要平均一年,但可能需要长达四年,一个人的免疫系统,以控制最初的感染。在此期间的筛查可能显示这种免疫反应和修复为轻度异常,这通常与宫颈癌无关,但可能导致患者压力并导致进一步的测试和可能的治疗。宫颈癌通常需要一段时间才能发展,因此延迟几年的筛查开始几乎不会有遗漏潜在癌前病变的风险。例如,筛查25岁以下的人不会降低30岁以下的癌症发病率。
筛查没有性接触的人很少或根本没有好处。例如,美国预防服务工作组(USPSTF)建议在第一次性行为后至少等待三年。 HPV可以在女性之间进行性交,所以那些只与其他女性发生性关系的人应该接受筛查,尽管他们患宫颈癌的风险要低一些。
筛查频率指南各不相同 - 通常每三到五年一次,对于那些以前没有异常涂片的人。一些较旧的建议建议每隔一到两年进行一次筛查,但几乎没有证据支持这种频繁的筛查;年度筛查几乎没有什么好处,但会导致成本大大增加,许多不必要的程序和治疗。自1980年以来,人们已经认识到大多数人可以不经常筛查。在某些指南中,频率取决于年龄;例如在英国,对于50岁以下的女性,建议每3年进行一次筛查,对于那些超过50岁的女性,每5年进行一次。
筛查应该在65岁左右停止,除非最近有异常的检查或疾病。对于年龄在60岁或以上且之前的测试结果为阴性的人,可能没有任何福利筛查。根据USPSTF,ACOG,ACS和ASCP,如果女性的最后三次Pap结果正常,她可以在65岁时停止;英国的NHS说64.在完全子宫切除术治疗良性疾病后,没有必要继续进行筛查。
对于接种过HPV疫苗的人,仍建议进行子宫颈抹片检查筛查,因为疫苗不包括可导致宫颈癌的所有HPV类型。此外,疫苗在接种疫苗前不能预防HPV暴露。
那些有子宫内膜癌史的人应该停止常规的巴氏试验。进一步的检测不太可能检测到癌症的复发,但确实会带来假阳性结果的风险,这将导致不必要的进一步检测。
在异常的子宫颈抹片检查后,或在治疗异常的Pap或活组织检查结果后,或在治疗癌症后,可能需要更频繁的子宫颈抹片检查。
效用
巴氏试验与常规筛查和适当随访相结合,可使宫颈癌死亡率降低多达80%。
由于许多原因,可能出现通过巴氏试验预防癌症的失败,包括没有定期筛查,缺乏对异常结果的适当随访,以及取样和解释错误。在美国,超过一半的侵袭性癌症发生在从未接受子宫颈抹片检查的女性身上;另外10%至20%的癌症发生在前五年未接受过子宫颈抹片检查的患者中。大约四分之一的美国宫颈癌患者的宫颈抹片检查异常,但没有得到适当的随访(患者没有返回护理,或者临床医生没有进行推荐的检查或治疗)。
巴氏试验未发现子宫颈腺癌被预防。在英国,有子宫颈抹片检查筛查计划,腺癌约占所有宫颈癌的15%
对英国呼叫和召回系统有效性的估计差异很大,但它可能会阻止英国每年约700人死亡。每年进行200次测试的医生将在38年内防止一次死亡,同时看到152名患者的结果异常,参考调查79次,获得53次异常活检结果,并且看到17次持续异常持续超过两年。尽管经过筛选,38年内至少有一名女性会死于宫颈癌。
由于英国人口约为6100万,因此在英国接受子宫颈抹片检查的最大人数约为1500万至2000万(消除了20岁以下和65岁以上人口的百分比)。这表明在英国使用子宫颈抹片检查可以为大约20,000名接受检测的女性(假设每年测试15,000,000名女性)挽救1名女性的生命。如果每年实际测试的数量仅为10,000,000,那么对于每15,000名接受测试的女性来说,这样可以挽救1名女性的生命。
结果
在筛查一般或低风险人群时,大多数Pap结果是正常的。
在美国,每年发现大约2-3百万个异常子宫颈抹片检查结果。大多数异常结果是轻度异常(ASC-US(通常为Pap结果的2-5%)或低度鳞状上皮内病变(LSIL)(约占结果的2%)),表明HPV感染。[引证需要]尽管最低宫颈发育不良自发消退而不会导致宫颈癌,发育不良可以作为需要提高警惕性的指示。
在一个典型的情况下,大约0.5%的Pap结果是高级SIL(HSIL),不到0.5%的结果表明癌症; 0.2至0.8%的结果表明未确定意义的非典型腺细胞(AGC-NOS)。
随着基于液体的制剂(LBP)成为测试的常用介质,非典型结果率增加。使用LBP的所有低度鳞状上皮内病变制剂的中位率为2.9%,而2003年的中位率为2.1%。高级别鳞状上皮内病变(中位数,0.5%)和非典型鳞状细胞的发生率变化不大。
根据Bethesda系统报告了异常结果。他们包括:
鳞状细胞异常(SIL)
意义不明的非典型鳞状细胞(ASC-US)
非典型鳞状细胞 - 不能排除HSIL(ASC-H)
低度鳞状上皮内病变(LGSIL或LSIL)
高度鳞状上皮内病变(HGSIL或HSIL)
鳞状细胞癌
腺上皮细胞异常
未另行规定的非典型腺细胞(AGC或AGC-NOS)
也可以检测到宫颈内膜和子宫内膜异常,以及包括酵母,单纯疱疹病毒和毛滴虫病在内的许多感染过程。 然而,它在检测这些感染时不是非常敏感,因此在Pap上没有检测并不意味着没有感染。
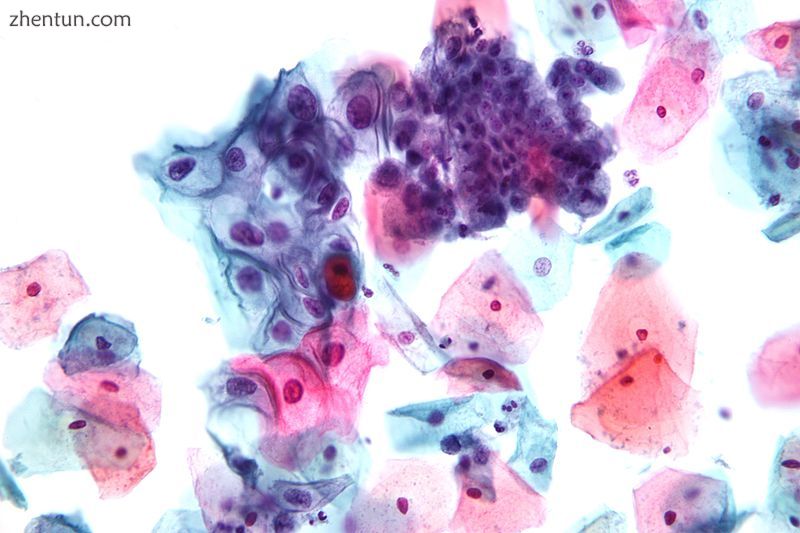
巴氏试验的显微照片显示低级别上皮内病变(LSIL)和良性宫颈内膜粘膜。 巴氏染色。
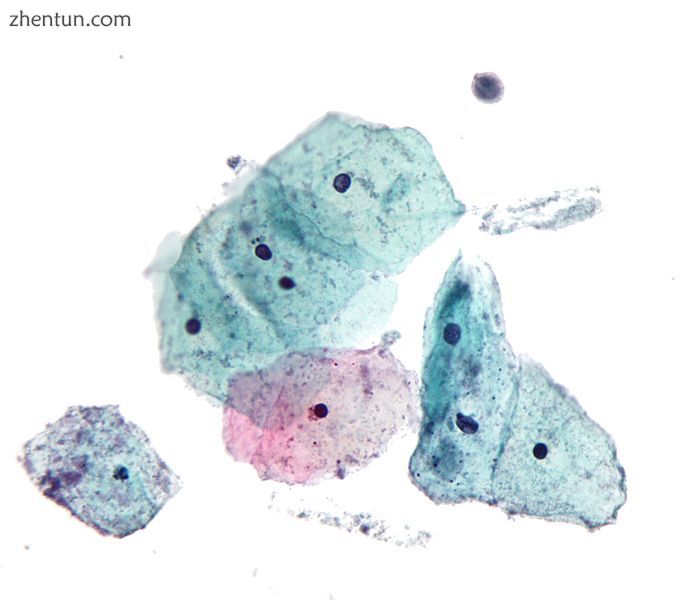
显示毛滴虫病的巴氏试验的显微照片。 在右上角看到的滴虫有机体。 巴氏染色。
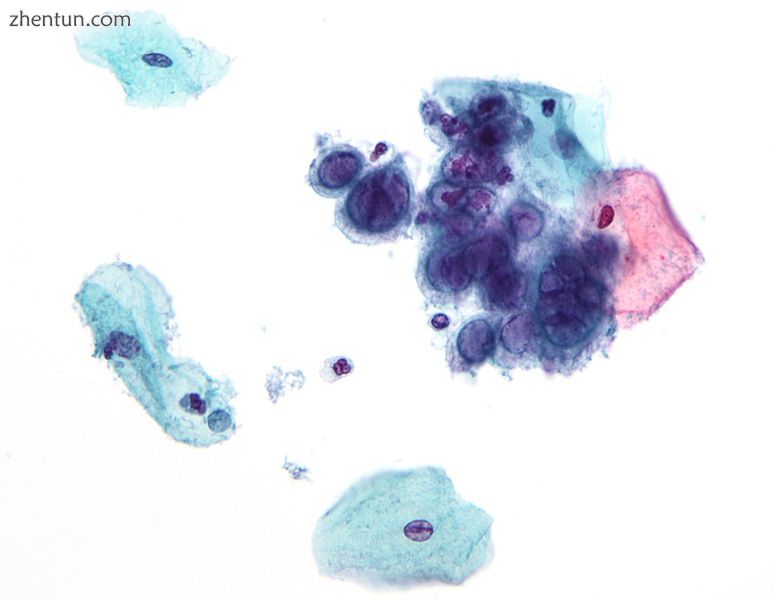
巴氏试验的显微照片显示单纯疱疹病毒的变化。 巴氏染色。
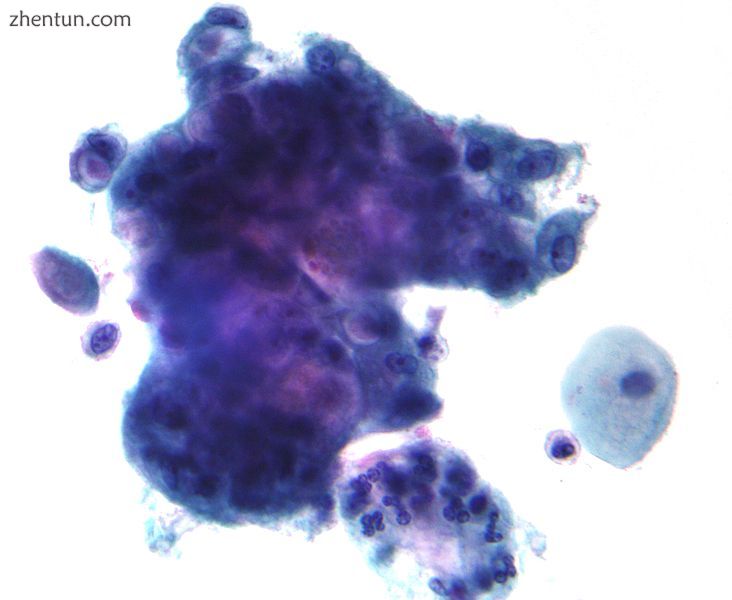
子宫颈腺癌在pap测试。
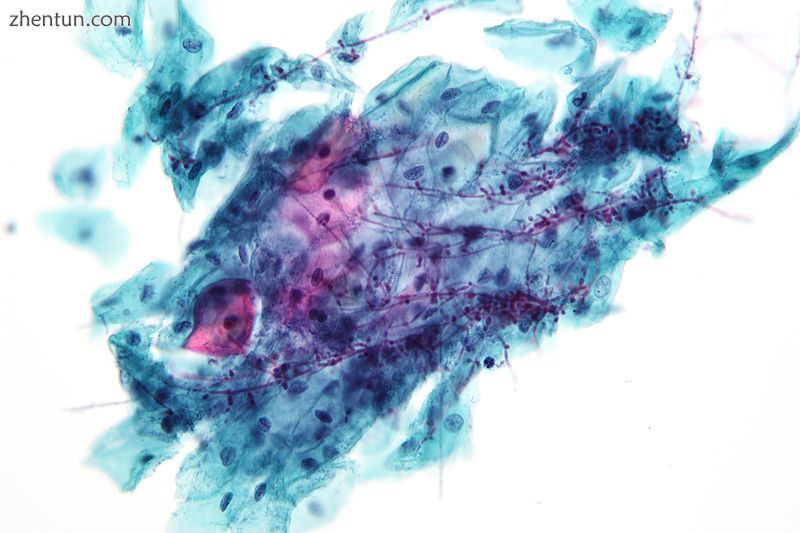
在pap测试的念珠菌有机体。
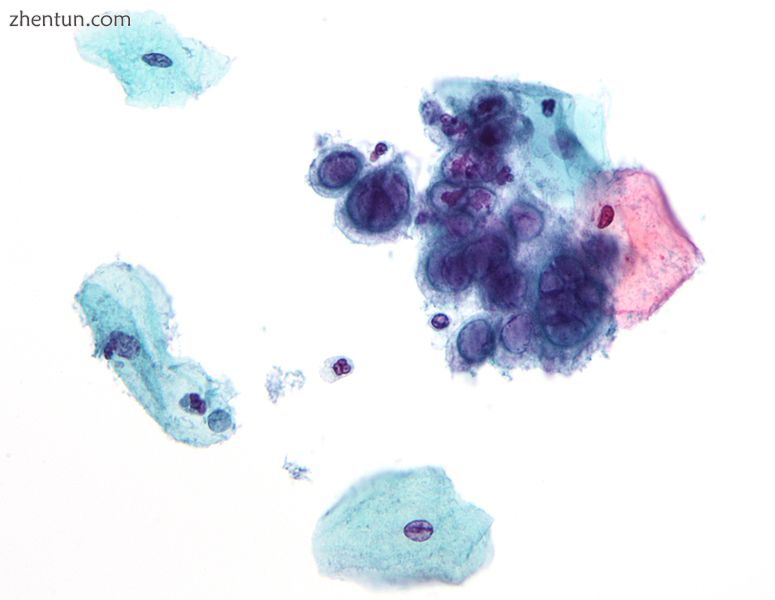
病毒性细胞病变效应与pap单纯疱疹病毒一致。
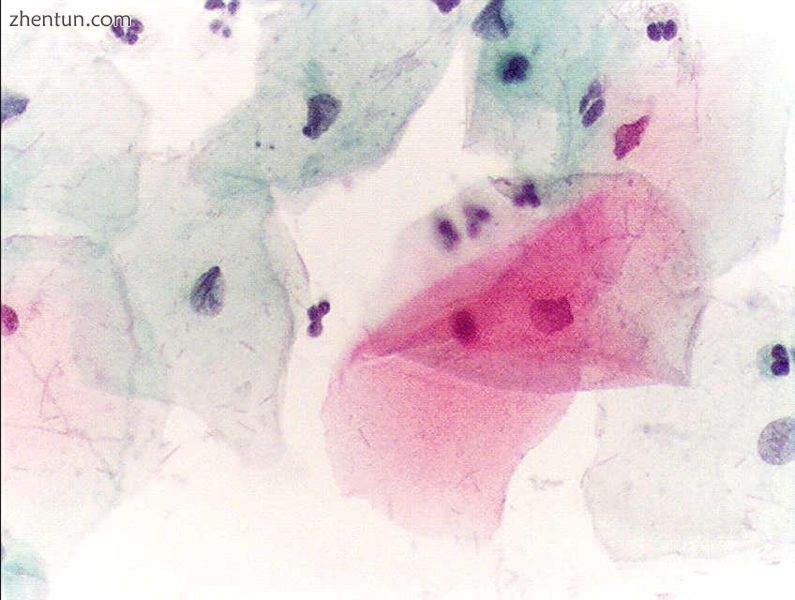
绝经前妇女的正常鳞状上皮细胞
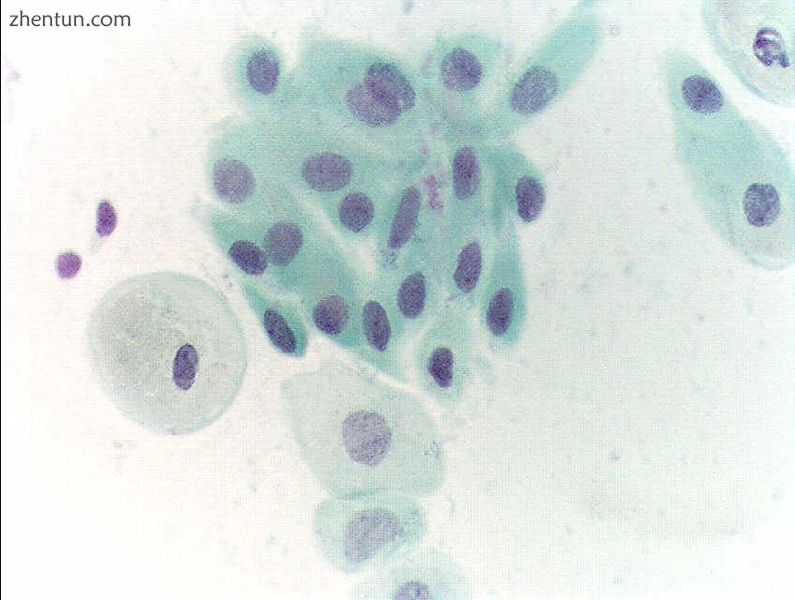
绝经后妇女的萎缩性鳞状细胞
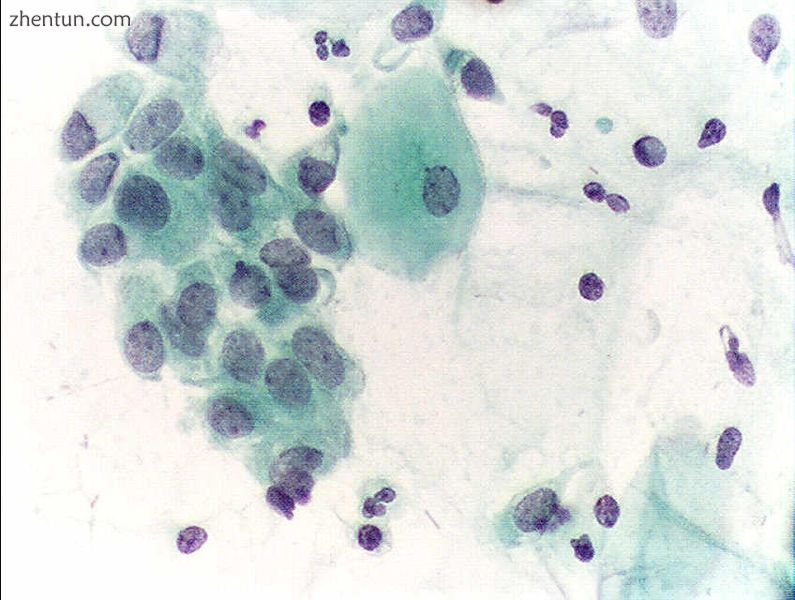
正常的宫颈内细胞应该存在于载玻片中,作为高质量取样的证据
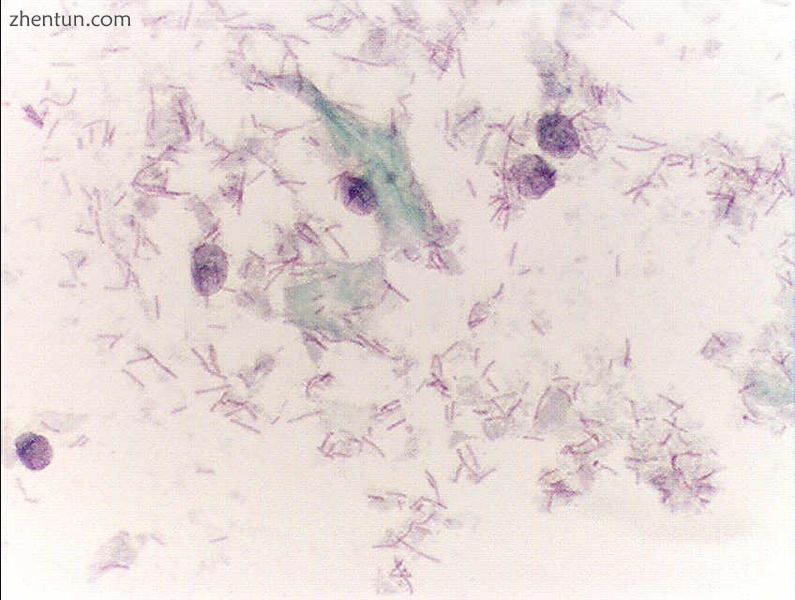
鳞状上皮细胞的细胞质融化了; 可以看到许多Döderlein杆菌
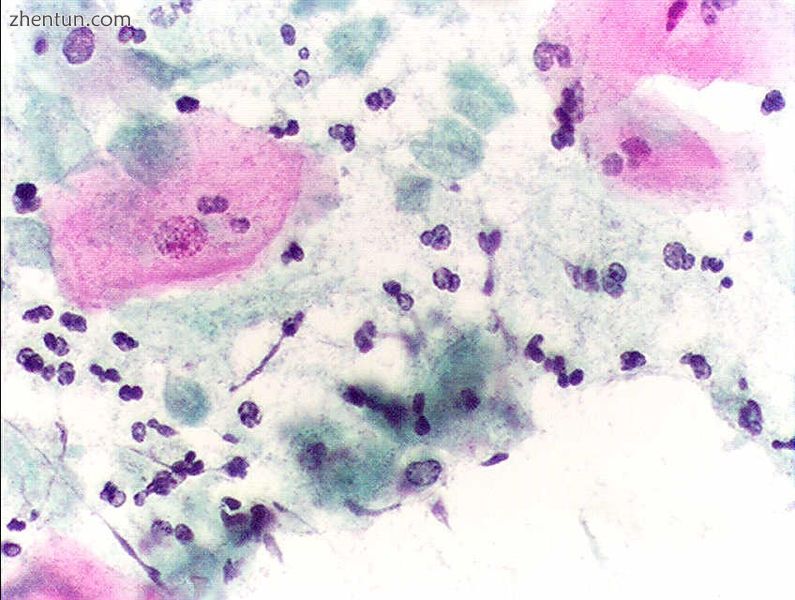
阴道毛滴虫感染
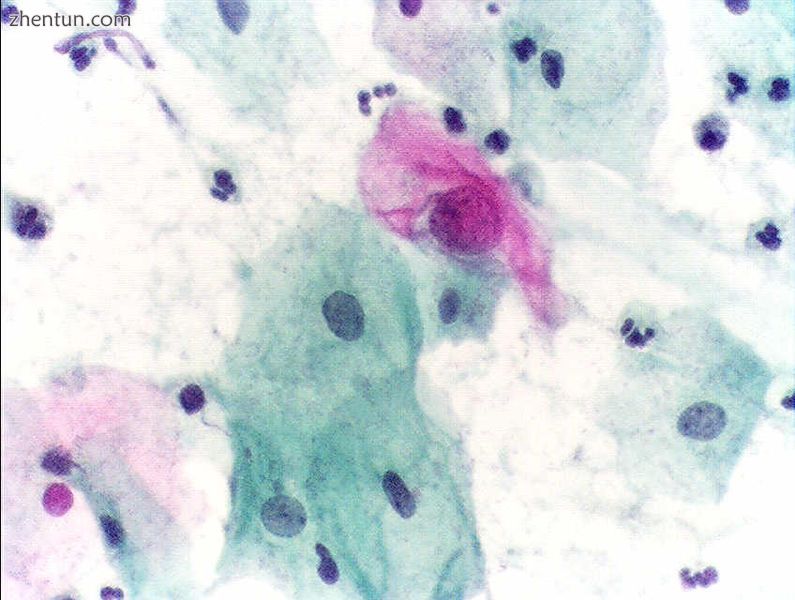
可以看到明显不典型的细胞
怀孕
巴氏试验通常可以在怀孕期间进行,直至至少24周的孕龄。 怀孕期间的巴氏试验与流产风险增加无关。 在孕妇的子宫颈抹片检查中常见炎症成分,并且似乎没有后续早产的风险。
分娩后,建议在进行pap检测前等待12周,因为分娩引起的子宫颈炎症会干扰检测。
程序
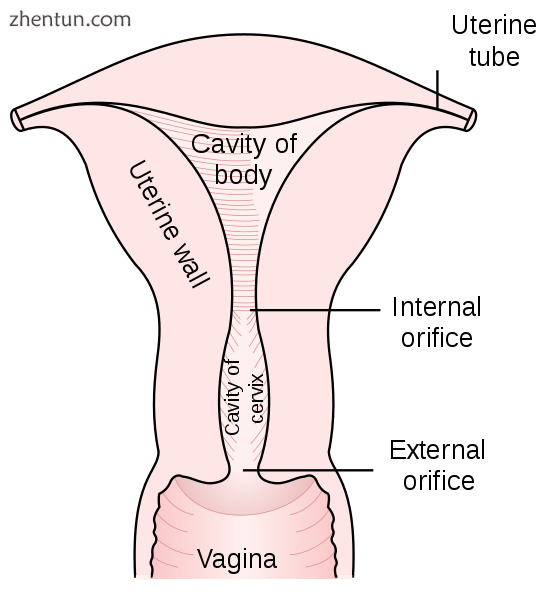
子宫颈与阴道上部和子宫后部有关。
为了获得最佳效果,女性月经期间不应进行巴氏试验,部分原因是额外的细胞可能使宫颈细胞模糊,部分原因是月经周期的这一部分是女性器官发炎最多/ LINK /。然而,子宫颈抹片检查可以在女性月经期间进行,特别是如果医生正在使用液体检测;如果出血非常重,子宫内膜细胞可能会遮盖宫颈细胞,因此如果出血过多则不宜进行子宫颈抹片检查。
获得子宫颈抹片检查不应该引起太多疼痛,但是如果妇女有某些未经治疗的阴道问题,例如颈椎管狭窄或阴道痉挛,或者如果执行它的人过于刺激,或使用错误尺寸的窥器,则可以。
然而,由于两个共同作用的原因,它们并不舒服:子宫颈充满伤害感受器,用于收集细胞的刷子必须足够硬,以便将它们从周围组织刮掉。所以它可能会让人感到不舒服,但通常很快,所获得的信息可能很关键。
患有潜在疼痛或组织疾病的人,如果需要,可以采取适当的预防措施,提前与他们的医疗服务提供者讨论过程中疼痛或组织疾病,这些疼痛或组织疾病会对伤害感受器(疼痛神经)被刮伤或过度感冒。一个较小的窥器,利多卡因凝胶,提前加热仪器和润滑剂,以及在检查室的额外时间和温和的技术,都可以有助于降低可管理水平的风险。这些是合理的要求,并与良好实践保持一致。
许多人之后会出现斑点或轻度腹泻。斑点通常来自宫颈刮伤,腹泻可能是由于在检查期间间接刺激下肠。
许多医疗保健提供者的错误印象是,只应使用无菌水或根本不使用润滑剂来润滑窥器。这可能导致不必要的不​​适。许多研究表明,使用少量水基凝胶润滑剂不会干扰,模糊或扭曲PAP涂片。此外,细胞学不受影响,也没有一些STD测试。
医护人员首先将窥器插入女性阴道,将阴道扩散开,并允许进入子宫颈。然后,医疗保健提供者通过用艾尔斯伯里刮刀刮擦子宫颈的外开口或口腔来收集细胞样本。子宫颈刷在子宫颈的中央开口中旋转。将细胞置于载玻片上并送至实验室检查其异常情况。
有时使用塑料扫帚代替抹刀和刷子。扫帚不是一个好的收集装置,因为它比收集刮刀和刷子的内宫颈材料收集效率低得多。随着基于液体的细胞学的出现,扫帚更频繁地使用,尽管任何类型的收集装置可以与任一类型的细胞学一起使用。
使用Papanicolaou技术对样品进行染色,其中通过细胞选择性地保留着色染料和酸。用光学显微镜看不到未染色的细胞。 Papanicolaou选择了突出细胞质角质化的染色剂,这实际上几乎与用于诊断的核特征无关。
在某些情况下,计算机系统可以预先筛选幻灯片,指示那些不需要人检查或突出显示特别注意区域的幻灯片。然后通常使用光学显微镜由经过专门培训且合格的细胞学技术人员筛选样品。筛选样本的术语因国家而异;在英国,人员被称为细胞分离器,生物医学科学家(BMS),高级从业者和病理学家。后两者负责报告可能需要进一步调查的异常样本。
自动分析
在过去十年中,已成功尝试开发用于筛选的自动化计算机图像分析系统。虽然根据现有证据,不能建议将自动化宫颈筛查纳入国家筛查计划,但最近的NHS健康技术评估结论认为“可能已经进行了自动化图像分析的一般情况(d)。”自动化可以提高灵敏度并减少不令人满意的标本。两个系统已获得FDA批准,并在大批量参考实验室中发挥作用,并进行人为监督。
筛选类型
对于其他宫颈筛查试验和人乳头瘤病毒检测,请参见宫颈筛查。
传统的巴氏涂片 - 在传统的巴氏涂片中,样品在收集后直接涂抹在显微镜载玻片上。
液基细胞学 - (上皮细胞)样本取自过渡区;子宫颈的鳞状柱状交界处,在外部和子宫颈之间。液基细胞学通常使用箭形刷,而不是传统的刮刀。将取出的细胞悬浮在一瓶防腐剂中以运输到实验室,在那里使用Pap染色剂进行分析。
巴氏试验通常寻找上皮异常/化生/异常增生/临界变化,所有这些都可能是CIN的指征。细胞核会染成深蓝色,鳞状细胞会染成绿色,角质细胞会染成粉红色/橙色。在存在一些(上皮细胞)异常的情况下可以观察到细胞。挖空细胞中的细胞核通常是不规则的,这表明可能引起关注;需要进一步确认屏幕和测试。
此外,人乳头状瘤病毒(HPV)测试可以按照异常Pap结果的指示进行,或者在某些情况下进行双重测试,其中Pap涂片和HPV测试同时进行(也称为Pap co-测试)。
实践方面
可以使用用于获得宫颈外膜样本的装置对子宫颈内部进行部分取样,但是由于该区域的解剖结构,不能保证一致且可靠的取样。由于可以对异常的宫颈内细胞进行取样,因此教导他们检查它们。
使用用于对宫外膜进行取样的装置不直接取样子宫内膜。细胞可能会剥落到子宫颈上并从那里收集,因此宫颈内细胞可以识别异常细胞(如果存在),但不应将巴氏试验用作子宫内膜恶性肿瘤的筛查工具。
在美国,pap测试本身花费20到30美元,但pap测试访问的成本可能超过1000美元,主要是因为增加了可能需要或可能不需要的额外测试。
历史
该测试由着名的希腊裔美国医生Georgios Papanikolaou发明并以其命名,他于1923年开始研究。罗马尼亚的AurelBabeş在1927年独立地发现了类似的发现。然而,Babeş的方法与Papanicolaou法截然不同。
Papanicolaou的名字一再被提交给诺贝尔委员会,并且每次都被拒绝。诺贝尔委员会将对Papanicolaou优缺点的深入调查授权给当时担任斯德哥尔摩癌症研究所(Radiumhemmet)病理学负责人的桑特森教授。 Santesson发现Babeş的贡献从未被Papanicolaou引用,并且正式向委员会报告了这一事实,委员会随后拒绝了Papanicolaou的诺贝尔奖。
实验技术
在发达国家,阴道镜检查引导的宫颈活检被认为是诊断异常子宫颈抹片检查后宫颈异常的“金标准”。其他技术如三重涂片也在异常子宫颈抹片检查后进行。该程序需要训练有素的colposcopist,并且执行起来可能很昂贵。然而,子宫颈抹片检查非常敏感,一些阴性活检结果可能代表活组织检查中病变的欠采样,因此细胞学阳性的阴性活检需要仔细跟进。
实验可视化技术使用宽带光(例如,直接可视化,透视检查,宫颈造影,用乙酸或用Lugol和阴道镜检查进行目视检查)和电子检测方法(例如,Polarprobe和体内光谱法)。这些技术成本较低,并且可以在极少的培训下进行。它们的表现不如子宫颈抹片检查和阴道镜检查。此时,这些技术尚未通过大规模试验验证,并且一般不使用。
访问
        
本节需要扩展:全球范例,不太关注世界上两个选择性区域。您可以通过添加它来提供帮助。 (2017年1月)
在台湾,大多数中产阶级和上层阶级的人都可以参加巴氏试验,并且可以选择每年完成一次。另一方面,像美国南部研究中的那些穷人可能并不总是能够接受巴氏试验。
球菌细菌
在pap测试中发现的球菌细菌与其他正常的测试结果无关,也没有传染性症状。然而,如果有足够的炎症来掩盖癌前和癌症过程的检测,则可能表明在重复涂片之前用链球菌和厌氧菌(如甲硝唑和阿莫西林)用广谱抗生素治疗。或者,测试将在比其他情况更早的时间重复进行。如果出现阴道分泌物,恶臭或刺激症状,球菌细菌的存在也可能表明如上所述用抗生素治疗。
参考
"Pap Smear: MedlinePlus Lab Test Information". medlineplus.gov. Retrieved 2018-11-07.
"Cervical Screening". NHS. Retrieved 2018-09-04.
Moyer, VA; U.S. Preventive Services Task, Force (Jun 19, 2012). "Screening for cervical cancer: U.S. Preventive Services Task Force recommendation statement". Annals of Internal Medicine. 156 (12): 880–91, W312. doi:10.7326/0003-4819-156-12-201206190-00424. PMID 22711081.
Saslow, D; et al. (2012). "American Cancer Society, American Society for Colposcopy and Cervical Pathology, and American Society for Clinical Pathology Screening Guidelines for the Prevention and Early Detection of Cervical Cancer" (PDF). Journal of Lower Genital Tract Disease. 16 (3).
American Cancer Society. (2010). Detailed Guide: Cervical Cancer. Can cervical cancer be prevented? Retrieved August 8, 2011.
The American College of Obstetricians and Gynecologists (2009). "ACOG Education Pamphlet AP085 – The Pap Test". Washington, DC. Archived from the original on June 15, 2010. Retrieved June 5, 2010.
Shidham, VinodB; Mehrotra, Ravi; Varsegi, George; D′Amore, KristaL; Hunt, Bryan; Narayan, Raj (2011-01-01). "p16 INK4a immunocytochemistry on cell blocks as an adjunct to cervical cytology: Potential reflex testing on specially prepared cell blocks from residual liquid-based cytology specimens". CytoJournal. 8 (1). doi:10.4103/1742-6413.76379. PMC 45765. PMID 21369522.
U.S. Preventive Services Task Force (2003). "Screening for Cervical Cancer: Recommendations and Rationale. AHRQ Publication No. 03-515A". Rockville, MD.: Agency for Healthcare Research and Quality. Retrieved June 5, 2010.
U.S. Preventive Services Task Force (March 2012). "Screening for Cervical Cancer: Clinical Summary of USPSTF Recommendation". uspreventiveservicestaskforce.org. Retrieved 31 July 2012.
American Academy of Family Physicians. "Five Things Physicians and Patients Should Question" (PDF). Choosing Wisely: an initiative of the ABIM Foundation. American Academy of Family Physicians. Retrieved August 14, 2012{{inconsistent citations}}
Arbyn M, Anttila A, Jordan J, Ronco G, Schenck U, Segnan N, Wiener H, Herbert A, von Karsa L (2010). "European Guidelines for Quality Assurance in Cervical Cancer Screening. Second Edition—Summary Document". Annals of Oncology. 21 (3): 448–458. doi:10.1093/annonc/mdp471. PMC 2826099. PMID 20176693.
Strander B (2009). "At what age should cervical screening stop?". Br Med J. 338: 1022–23. doi:10.1136/bmj.b809. PMID 19395422.
Sasieni P, Adams J, Cuzick J (2003). "Benefit of cervical screening at different ages: evidence from the UK audit of screening histories". Br J Cancer. 89 (1): 88–93. doi:10.1038/sj.bjc.6600974. PMC 2394236. PMID 12838306.
Society of Gynecologic Oncology (February 2014). "Five Things Physicians and Patients Should Question". Choosing Wisely: an initiative of the ABIM Foundation. Society of Gynecologic Oncology. Retrieved 19 February 2013{{inconsistent citations}}, which cites
Salani R, Backes FJ, Fung MF, Holschneider CH, Parker LP, Bristow RE, Goff BA (2011). "Posttreatment surveillance and diagnosis of recurrence in women with gynecologic malignancies: Society of Gynecologic Oncologists recommendations". American Journal of Obstetrics and Gynecology. 204 (6): 466–78. doi:10.1016/j.ajog.2011.03.008. PMID 21752752.
Salani R, Nagel CI, Drennen E, Bristow RE (2011). "Recurrence patterns and surveillance for patients with early stage endometrial cancer". Gynecologic Oncology. 123 (2): 205–7. doi:10.1016/j.ygyno.2011.07.014. PMID 21820709.
Bristow RE, Purinton SC, Santillan A, Diaz-Montes TP, Gardner GJ, Giuntoli RL (2006). "Cost-effectiveness of routine vaginal cytology for endometrial cancer surveillance". Gynecologic Oncology. 103 (2): 709–13. doi:10.1016/j.ygyno.2006.05.013. PMID 16797686.
"ACOG Committee on Gynecologic Practice; Routine Pelvic Examination and Cervical Cytology Screening, Opinion #413". Obstetrics and Gynecology. 113 (5): 1190–1193. 2009. doi:10.1097/AOG.0b013e3181a6d022. PMID 19384150.
American Congress of Obstetricians and Gynecologists. "Five Things Physicians and Patients Should Question". Choosing Wisely: an initiative of the ABIM Foundation. American Congress of Obstetricians and Gynecologists. Retrieved August 1, 2013., which cites
Boulware LE, Marinopoulos S, Phillips KA, Hwang CW, Maynor K, Merenstein D, Wilson RF, Barnes GJ, Bass EB, Powe NR, Daumit GL (2007). "Systematic review: The value of the periodic health evaluation". Annals of Internal Medicine. 146 (4): 289–300. doi:10.7326/0003-4819-146-4-200702200-00008. PMID 17310053.
Saslow D, Solomon D, Lawson HW, Killackey M, Kulasingam SL, Cain J, Garcia FA, Moriarty AT, Waxman AG, Wilbur DC, Wentzensen N, Downs LS, Spitzer M, Moscicki AB, Franco EL, Stoler MH, Schiffman M, Castle PE, Myers ER (2012). "American Cancer Society, American Society for Colposcopy and Cervical Pathology, and American Society for Clinical Pathology screening guidelines for the prevention and early detection of cervical cancer". CA Cancer J Clin. 62 (3): 147–72. doi:10.3322/caac.21139. PMC 3801360. PMID 22422631.
"Committee Opinion No. 534". Obstetrics & Gynecology. 120 (2, Part 1): 421–424. 2012. doi:10.1097/AOG.0b013e3182680517. PMID 22825111.
"ACOG Practice Bulletin Number 131: Screening for cervical cancer". Obstetrics and gynecology. 120 (5): 1222–1238. 2012. doi:10.1097/AOG.0b013e318277c92a. PMID 23090560.
"Can Cervical Cancer Be Prevented?". www.cancer.org. Retrieved 2018-11-07.
Sasieni, P; Castanon, A; Cuzick, J; Snow, J (2009). "Effectiveness of Cervical Screening with Age: Population based Case-Control Study of Prospectively Recorded Data". BMJ. 339: 2968–2974. doi:10.1136/bmj.b2968.
Marrazzo JM, Koutsky LA, Kiviat NB, Kuypers JM, Stine K (2001). "Papanicolaou test screening and prevalence of genital human papillomavirus among women who have sex with women". American Journal of Public Health. 91 (6): 947–952. doi:10.2105/AJPH.91.6.947. PMC 1446473. PMID 11392939.
Smith, RA; et al. (2002). "American Cancer Society Guideline for the Early Detection of Cervical Neoplasia and Cancer". 52 (1): 8–22. ACS and others have recommended, since before 1980, that conventional cytology can be safely performed up to every three years for most women.
DeMay, M. (2007). Practical principles of cytopathology. Revised edition. Chicago, IL: American Society for Clinical Pathology Press. ISBN 978-0-89189-549-7.
"Cancer Research UK website". Archived from the original on 2009-01-16. Retrieved 2009-01-03.
Raffle AE, Alden B, Quinn M, Babb PJ, Brett MT (2003). "Outcomes of screening to prevent cancer: analysis of cumulative incidence of cervical abnormality and modelling of cases and deaths prevented". BMJ. 326 (7395): 901. doi:10.1136/bmj.326.7395.901. PMC 153831. PMID 12714468.
"Pap Smear". Retrieved 2008-12-27.
Eversole GM, Moriarty AT, Schwartz MR, Clayton AC, Souers R, Fatheree LA, Chmara BA, Tench WD, Henry MR, Wilbur DC (2010). "Practices of participants in the college of american pathologists interlaboratory comparison program in cervicovaginal cytology, 2006". Archives of Pathology & Laboratory Medicine. 134 (3): 331–5. doi:10.1043/1543-2165-134.3.331. PMID 20196659.
Nayar, Ritu; Solomon, Diane (2004-01-01). "Second edition of 'The Bethesda System for reporting cervical cytology' - Atlas, website, and Bethesda interobserver reproducibility project". CytoJournal. 1 (1): 4. doi:10.1186/1742-6413-1-4. PMC 526759. PMID 15504231.
PapScreen Victoria > Pregnant women Archived 2014-02-01 at the Wayback Machine. from Cancer Council Victoria 2014
[1] Michael CW (1999). "The Papanicolaou Smear and the Obstetric Patient: A Simple Test with Great Benefits". Diagnostic Cytopathology. 21 (1): 1–3. doi:10.1002/(SICI)1097-0339(199907)21:1<1::AID-DC1>3.0.CO;2-0. PMID 10405797.
Lanouette JM, Puder KS, Berry SM, Bryant DR, Dombrowski MP (1997). "Is inflammation on Papanicolaou smear a risk factor for preterm delivery?". Fetal Diagnosis and Therapy. 12 (4): 244–247. doi:10.1159/000264477. PMID 9354886.
"Pregnant women". papscreen.org. Cancer Council Victoria. Archived from the original on 2015-01-08. Retrieved 2015-01-16.
"Excerpts from Changing Bodies, Changing Lives". Our Bodies Ourselves. Archived from the original on 2013-12-18. Retrieved 2013-07-02.
Tingåker, Berith K; Irestedt, Lars (2010). "Changes in uterine innervation in pregnancy and during labour". Current Opinion in Anesthesiology. 23 (3): 300–303. doi:10.1097/aco.0b013e328337c881. PMID 20216064.
Wright, Jessica L. (2010). "The Effect of Using Water-based Gel Lubricant During a Speculum Exam On Pap Smear Results". School of Physician Assistant Studies. Pacific University. Retrieved 4 February 2012.
Martin-Hirsch P, Lilford R, Jarvis G, Kitchener HC (1999). "Efficacy of cervical-smear collection devices: a systematic review and meta-analysis". Lancet. 354 (9192): 1763–1770. doi:10.1016/S0140-6736(99)02353-3. PMID 10577637.
Biscotti CV, Dawson AE, Dziura B, Galup L, Darragh T, Rahemtulla A, Wills-Frank L (2005). "Assisted primary screening using the automated ThinPrep Imaging System". Am. J. Clin. Pathol. 123 (2): 281–7. doi:10.1309/AGB1MJ9H5N43MEGX. PMID 15842055.
Willis BH, Barton P, Pearmain P, Bryan S, Hyde C, "Cervical screening programmes: can automation help? Evidence from systematic reviews, an economic analysis and a simulation modelling exercise applied to the UK". Health Technol Assess 2005 9(13).[2] Archived 2008-09-10 at the Wayback Machine.
Davey E, d'Assuncao J, Irwig L, Macaskill P, Chan SF, Richards A, Farnsworth A (2007). "Accuracy of reading liquid based cytology slides using the ThinPrep Imager compared with conventional cytology: prospective study". BMJ. 335 (7609): 31. doi:10.1136/bmj.39219.645475.55. PMC 1910624. PMID 17604301.
https://www.cancer.gov/types/cervical/pap-hpv-testing-fact-sheet
Bettigole C (2013). "The Thousand-Dollar Pap Smear". New England Journal of Medicine. 369 (16): 1486–1487. doi:10.1056/NEJMp1307295. PMID 24131176.
M.J. O'Dowd, E.E. Philipp, The History of Obstetrics & Gynaecology, London, Parthenon Publishing Group, 1994, p. 547.
Diamantis A, Magiorkinis E, Androutsos G (Jul 2010). "What's in a name? Evidence that Papanicolaou, not Babeș, deserves credit for the Pap test". Diagn Cytopathol. 38 (7): 473–6. doi:10.1002/dc.21226.
Koss, Leopold G. (2003-01-01). "Aurel Babeş". International Journal of Gynecological Pathology. 22 (1): 101–102. doi:10.1097/00004347-200301000-00020. ISSN 0277-1691. PMID 12496707.
Krunger, TF; Botha, MH (2007). Clinical gynaecology (3 ed.). South Africa: Juta. p. 23. Retrieved 7 December 2016.
Bewtra, Chhanda; Pathan, Muhammad; Hashish, Hisham (2003-10-01). "Abnormal Pap smears with negative follow-up biopsies: Improving cytohistologic correlations". Diagnostic Cytopathology. 29 (4): 200–202. doi:10.1002/dc.10329. ISSN 1097-0339.
Fang-Hsin Leea; Chung-Yi Lic; Hsiu-Hung Wanga; Yung-Mei Yang (2013). "The utilization of Pap tests among different female medical personnel: A nationwide study in Taiwan". Preventive Medicine. 56 (6): 406–409. doi:10.1016/j.ypmed.2013.03.001. Retrieved September 20, 2013.
http://web.ebscohost.com/ehost/p ... 1&vid=2&hid=127#944 (see Tables 3 and 4)[dead link]
NB Peterson; HJ Murff; Y Cui; M Hargreaves; JH Fowke (Jul–Aug 2008). "Papanicolaou testing among women in the southern United States". Journal of Women's Health. 17 (6): 939–46. doi:10.1089/jwh.2007.0576. PMC 2942751. PMID 18582173. Retrieved October 15, 2013.
OB-GYN 101: Introductory Obstetrics & Gynecology > Coccoid Bacteria Archived 2014-02-22 at the Wayback Machine. by Michael Hughey Hughey at Texas Tech University Health Sciences Center. Retrieved Feb 2014. |